各位大同行小同行你们好,今天分享的文献是ACS NANO上的一篇文章,冷暴露疗法与一氧化氮(Nitric Oxide,NO)气体疗法联合放疗(Radiotherapy,RT)对乳腺癌的治疗效果研究,Cold Exposure Therapy Sensitizes Nanodrug-Mediated Radioimmunotherapy for Breast Cancer。
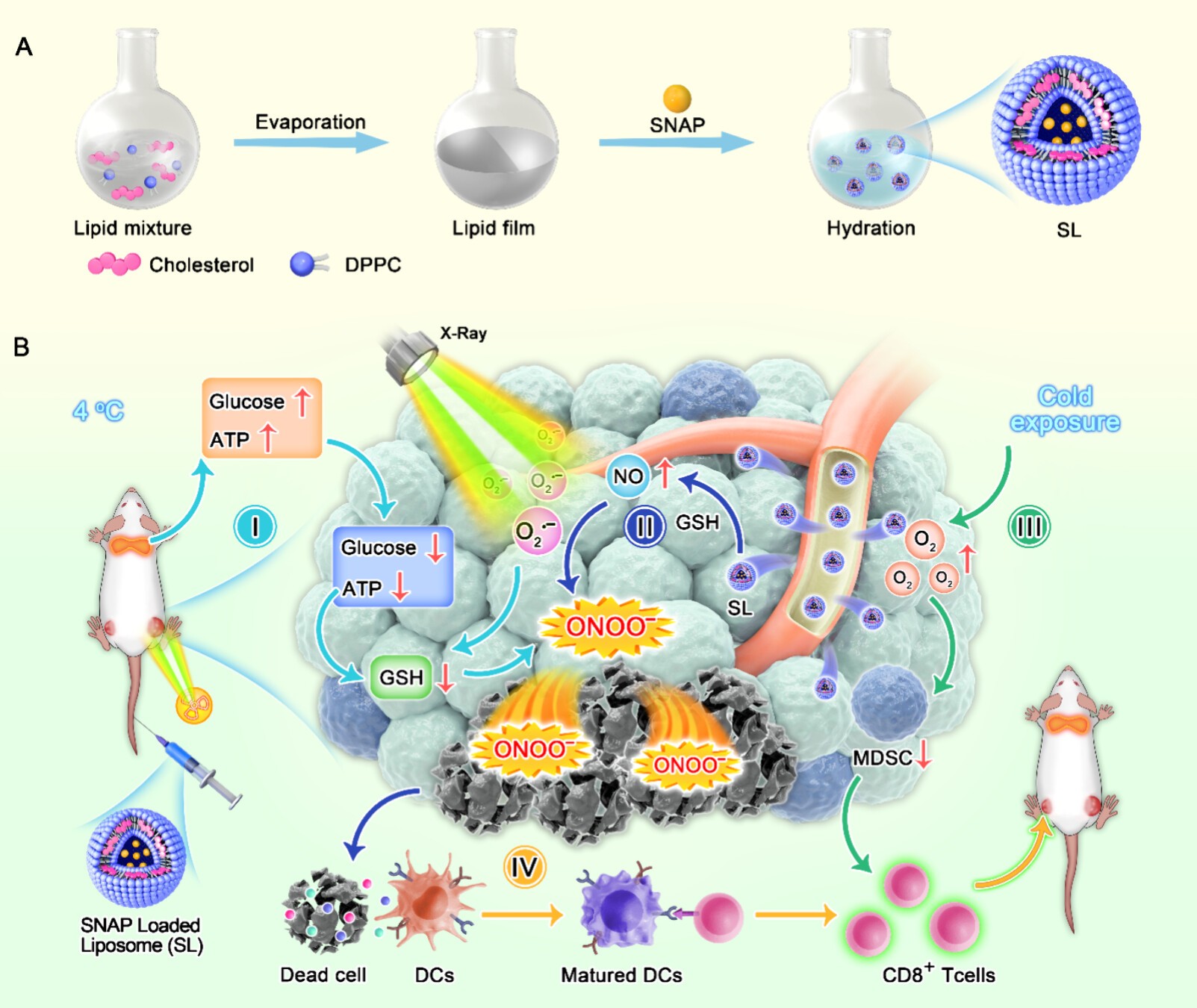
文章首先介绍了冷暴露疗法通过激活棕色脂肪组织(Brown Adipose Tissue,BAT)产热,迅速诱导肿瘤饥饿,探索了CE与传统疗法(如RT)联合使用的抗肿瘤机制。接着,研究人员构建了一种载有NO前药S-亚硝基-N-乙酰青霉素胺(SNAP)的脂质体(SL),在肿瘤区域内谷胱甘肽(GSH)的作用下释放NO,与RT产生的超氧阴离子反应生成具有强氧化性的过氧亚硝酸盐(ONOO−),诱导细胞死亡。
此外,小鼠在4°C的CE环境下,CE介导的BAT产热诱导肿瘤饥饿,降低了肿瘤内的ATP和GSH含量,改善了缺氧微环境,减少了骨髓源抑制细胞(MDSCs)。这些发现揭示了CE、NO气体疗法和RT的协同作用可能具有高效的抗癌效果,为个性化癌症治疗提供了可能性。
总结:
• 冷暴露疗法(CE)通过激活棕色脂肪组织(BAT)产热,迅速诱导肿瘤饥饿,与放疗(RT)和一氧化氮(NO)气体疗法联合使用,可增强肿瘤对RT的敏感性,并促进肿瘤的放射免疫疗法。
• 研究人员构建了一种载有NO前药SNAP的脂质体(SL),在肿瘤区域内GSH的作用下释放NO,与RT产生的超氧阴离子反应生成过氧亚硝酸盐(ONOO−),诱导细胞死亡,同时CE改善了肿瘤的缺氧微环境,降低了MDSCs,激活了全身抗肿瘤免疫。
• 该研究显示,CE、NO气体疗法和RT的联合治疗策略在抑制原发性肿瘤的同时,也能抑制远处肿瘤的生长,增强了抗肿瘤免疫反应,为癌症的个性化治疗提供了新的治疗途径。
评论:

